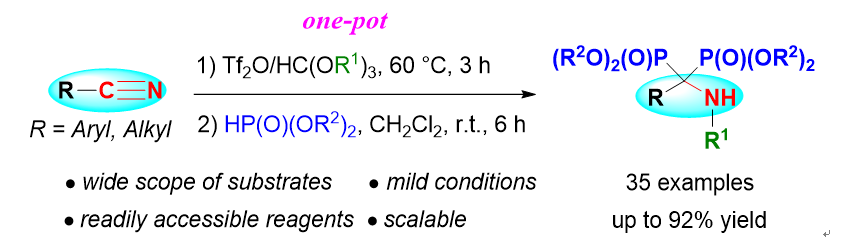
导语
α-氨基双膦酸(酯)类化合物(1-amino-1,1-bisphosphonates)是焦膦酸的类似物,具有代谢稳定的 P-C(N)-P 的骨架结构(图 1),因此和骨骼矿物质结合后可以长期留存,能够抑制骨细胞的生物化学靶点(FDPS/FPPS)活性,可用于治疗佩吉特病、骨质疏松症、高钙血症、多发性骨髓瘤等骨组织疾病。例如,Incadronate (1) 是目前治疗或预防骨质疏松症的药物之一。此外,这类化合物还具有抗真菌、抗氧化、抗肿瘤等广泛的生物活性。近日,厦门大学黄培强教授课题组报道了通过Tf2O/HC(OR)3介导的中断的类Ritter(里特)反应“一瓶”合成α-氨基双膦酸酯的新方法,相关成果在线发表于J. Org. Chem. (DOI: 10.1021/acs.joc.2c00718)
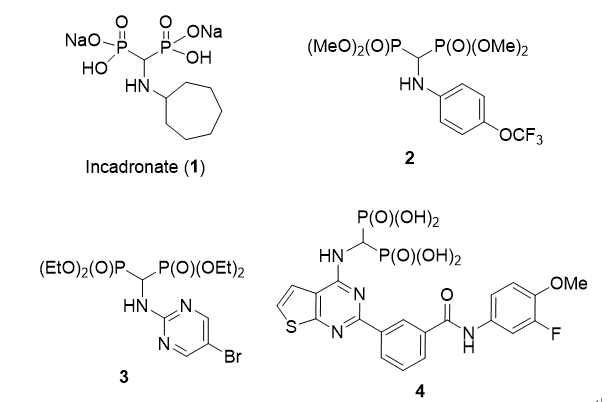
图1. 一些具有生物活性的α-氨基双膦酸酯类化合物
(来源:J. Org. Chem.)
前沿科研成果:通过Tf2O/HC(OR)3介导的中断的类Ritter反应合成α-氨基双膦酸酯
由于α-氨基双膦酸酯类化合物具有生物活性,其合成方法的研究一直为合成化学家所关注。在已报道的方法中,腈的双膦酰化是一种直接制备这类化合物的有效方法,如ZnCl2/Et3N或 Cp2TiCl2/Zn介导的腈与亚磷酸酯的反应,以及PCl3促进的腈与亚磷酸的缩合。另一方面,中断反应(Interrupt reaction)正获得越来越多的关注,通过捕获已知反应过程中形成的中间体来构建结构,生成新产物,使许多经典反应有了新的发展前景,日渐成为有用的化学合成工具。Ritter反应是从腈类化合物出发制备酰胺的高效途径之一,已广泛用于生物活性分子的合成。在Ritter反应中,腈与原位形成的叔或仲碳正离子(碳正离子通常来源于烯烃、醇及其衍生物)作用形成腈鎓中间体,然后水解生成酰胺。多种碳正离子等效体,如芳基重氮盐、N-乙烯基和N-芳基酰胺、三氟甲磺酸甲酯等也已被用于和腈作用形成腈鎓中间体。
黄培强教授课题组多年来致力于由仲酰胺生成腈鎓中间体的化学研究,通过与不同的亲核试剂反应构建新的碳碳键,实现了仲酰胺的多类直接高效转化(Angew. Chem. Int. Ed. 2012, 51, 8314;Org. Lett. 2015, 17, 732; Sci. Rep. 2016, 6, 28801; Org .Chem. Front. 2017, 4, 431;Org. Lett. 2019, 21, 1681; J. Org. Chem. 2021, 86, 5345)。在这些工作基础上,黄培强教授课题组又发展了一种从腈出发的基于中断的类Ritter反应的α-氨基双膦酸酯类化合物的“一瓶”合成方法:原位生成的TfOR1(由三氟甲磺酸酐和原甲酸酯反应生成)与腈作用生成腈鎓中间体,然后高反应性的腈鎓中间体与亚磷酸酯反应生成α-氨基双膦酸酯(图2)。
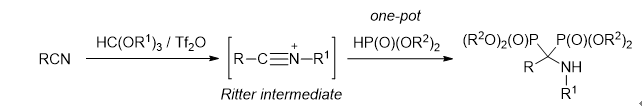
图2. 从腈出发合成α-氨基双膦酸酯类化合物
(来源:J. Org. Chem.)
作者以苯甲腈为底物进行条件优化,发现优化反应条件为:在室温下混合原甲酸三甲酯(0.6 equiv.)和Tf2O(0.6 equiv.)15分钟,加入腈在60°C下活化3小时,然后加入亚磷酸二乙酯(4.0 equiv.)和 CH2Cl2(0.5 M)并在室温下反应 6 小时。腈的底物适用性研究表明(图3),反应对于带有给电子基团的芳基腈均能给出较好的产率;带吸电子基团的芳基腈底物产率相对较低;苯环上取代基的位阻效应对反应有较明显的影响;反应对烷基腈底物也具良好的兼容性。值得一提的是,4-溴丁腈5w、5-溴戊腈5x在反应后得到的是自动环化产物6w、6x。并且,该反应可拓展至15 mmol规模,且产率没有明显下降(6a, 90% vs 87%)。另外,苯甲腈5a与亚磷酸二甲酯和亚磷酸二异丙酯、原甲酸乙酯均能顺利反应得到相应产物(图4)。
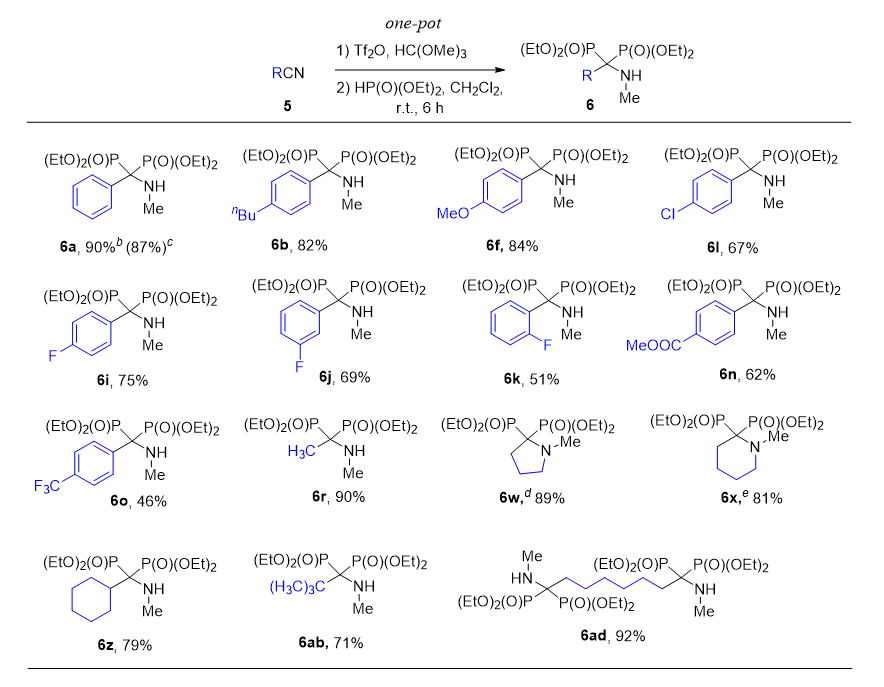
图3. 腈的底物拓展
(来源:J. Org. Chem.)
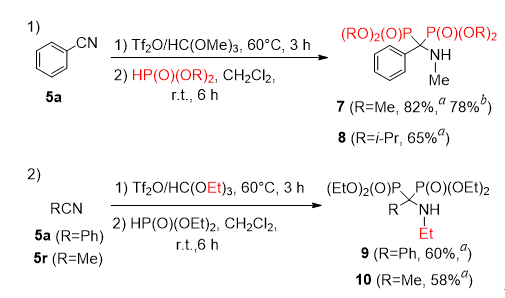
图4. 亚磷酸酯以及原甲酸酯的反应性
(来源:J. Org. Chem.)
另外,苯甲腈5a、仲烷基腈环己腈5z和叔烷基腈新戊腈5ab与Tf2O/HC(OMe)3作用生成腈鎓中间体后,再经TMSCN和亚磷酸二乙酯的连续处理,分别得到腈的氰基化/膦酰化产物α-氨基-α-氰基膦酸酯11a、11d、11e(图5)。然而,对于乙腈5r和丁腈5s,没有得到相应的产物α-氨基-α-氰基单膦酸酯11b和11c,得到的是双膦酰化产物6r和6s。
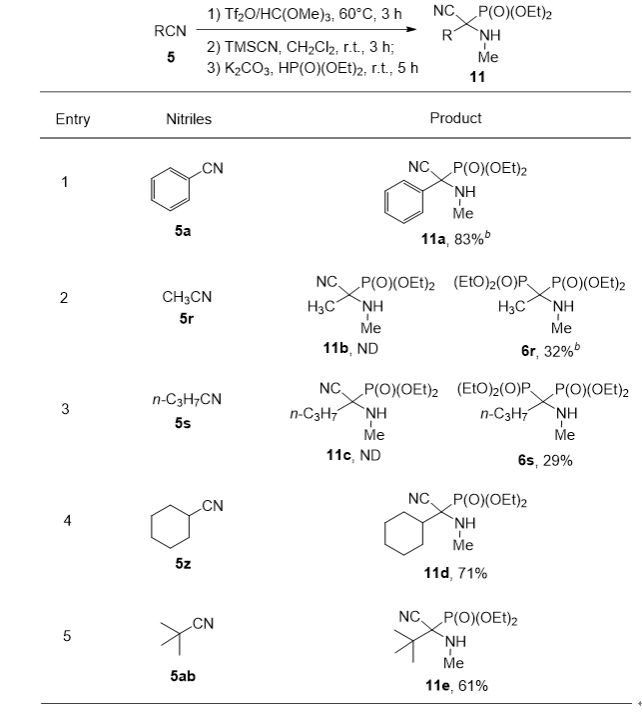
图5. 腈的氰基化/膦酰化反应
(来源:J. Org. Chem.)
作者还对所得的α-氨基双膦酸酯类化合物的13C NMR谱中丰富的31P-13C偶合进行了解析(图5),观察到特征性的跨越5根键的远程31P-13C偶合(6f),和跨越季碳和氮原子的3JP-C偶合(6f, 6s)。在苯环对位氟取代的产物6i的磷谱和氟谱中还观察到了罕见的跨越6根键的远程31P-19F偶合,但邻位、间位氟取代的产物6j, 6k中没有观察相应的5JP-F, 4JP-F偶合。
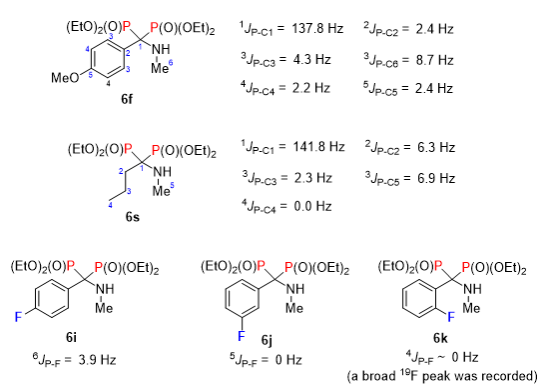
图5. 代表性的α-氨基双膦酸酯类化合物6f, 6s碳谱中观察到31P-13C偶合及化合物6i, 6j, 6k磷谱和氟谱中观察到的31P-19F偶合
综上所述,作者基于中断的类Ritter反应发展了一种从腈出发的简便且通用的α-氨基双膦酸酯类化合物合成方法。该方法具有广泛的底物适用性、无金属参与、条件温和等特点,且无需使用PCl3、Cp2TiCl2等有毒/敏感试剂。反应条件也可应用于腈的氰基化/膦酰化,得到α-氨基-α-氰基单膦酸酯产物。此外,在合成的α-氨基双膦酸酯中观察到少见的跨越5根键的远程5JP-C及跨越6根键6JP-F偶合。
上述工作以“One-Pot Synthesis of α-Amino Bisphosphonates from Nitriles via Tf2O/HC(OR)3‑Mediated Interrupted Ritter-Type Reaction”为题发表在J. Org. Chem. (DOI: 10.1021/acs.joc.2c00718)。课题组硕士研究生洪亚城为第一作者,叶剑良副教授和黄培强教授为共同通讯作者。该研究工作得到了国家重点研发计划(2017YFA0207302)、国家自然科学基金(21931010)的资助。
原文链接:
https://mp.weixin.qq.com/s/wILWb7t65Yt4OfK0R8RMAw